 |
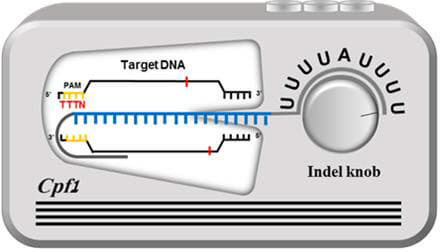
| CRISPR RNA의 유리디닐레이트의 추가를 통한 Cpf1의 유전자 교정 효율 증대를 표현한 모식도 |
CRISPR시스템은 잘못된 유전자를 교정해 유전자를 교정해 유전자치료에 사용할 수 있는 기술이다. CRISPR-Cas9이라는 3세대 유전자가위 기술의 개발로 유전자 편집 및 교정 분야의 기술이 급속도로 발전했다.
하지만 Cas9시스템은 크기가 크고, 원하는 타켓만 편집하는 기능(특이성)이 비교적 낮아 안전성이 문제가 될 수 있고, 급성 면역 거부반응을 일으키는 등 유전자치료에 있어 몇 가지 문제를 안고 있었다.
이에 반해 새로운 유전자가위인 Cpf1은 Cas9보다 상대적으로 작은 크기로 체내 전달이 쉽고 낮은 오프-타켓효과(비표적유전자를 교정하는 효과)를 가져 안정성이 높아, 특히 유전자 치료에 적합한 강점을 지닌다. 다만 유전자 교정 효율이 낮다는 유일한 단점을 가지고 있었다.
연구팀은 표적유전자와 결합하는 가이드 RNA의 말단을 엔지니어링해 Cas9이상의 교정효율을 갖는 유전자가위 기술을 확보했다. 별도의 화학적, 물리적 처리없이 간단한 방법을 통해 Cpf1의 강점인 작은 크기와 높은 안정성은 유지하면서 낮은 효율이라는 단점을 보완해 유전자 치료에 활용하기에 Cas9보다 더 나은 유전자 가위 기술로 발전시켰다.
또 Cas9과 Cpf1은 유전자치료를 할 수 있는 타켓에 대해 서로 보완의 관계에 있기 때문에 교정이 어렵던 유전자를 발전된 Cpf1으로 대체해 교정할 수 있어 유전자 가위의 선택성을 넓혔다고 할 수 있다.
이번 연구에서 사용된 엔지니어링은 매우 간단하고 저비용의 방법으로 구현할 수 있어 상용화에 유리하다.
또 바이러스 전달체를 사용한 유전자치료 발전에 기여할 것으로 예상된다. 황반 변성, 혈우병, 낭포성 섬유증과 같은 난치병에 대해 AAV 전달체 및 유전자 가위를 도입한 유전자 치료제가 개발되고 있어 고효율의 CRISPR-Cpf1 시스템의 적용 가능성이 기대된다.
김용삼 박사는 “Cpf1의 장점인 낮은 오프-타켓 효과는 유지하면서 간단한 방법으로 교정 효율을 올렸다는 것이 핵심”이라며 “AAV와 같은 바이러스 전달체를 이용한 유전자치료에 대한 활용 가능성이 높아졌다”고 밝혔다.
이해미 기자 ham7239@
중도일보(www.joongdo.co.kr), 무단전재 및 수집, 재배포 금지
 이해미 기자
이해미 기자

![[현장]구청·경찰 합동 쓰레기집 청소… 일부만 치웠는데 21톤 쏟아져](https://dn.joongdo.co.kr/mnt/webdata/content/2024y/11m/24d/118_2024112201001657300065231.jpg)



![[주말 사건사고] 청양 농업용 창고서 불…카이스트서 전동킥보드 화재](https://dn.joongdo.co.kr/mnt/webdata/content/2024y/11m/24d/78_2024112401001726300067831.jpg)
![[날씨] 12~1월 평년과 비슷하고 2월 따뜻](https://dn.joongdo.co.kr/mnt/webdata/content/2024y/11m/24d/78_2024112401001726800067861.jpg)



![[드림인대전]생존 수영 배우다 국가대표까지… 대전체고 김도연 선수](https://dn.joongdo.co.kr/mnt/images/webdata/content/2024y/11m/25d/2024112401001432800055941.jpg)





